LFSS 2020 : les mesures intéressant les pharmaciens
15/01/2020

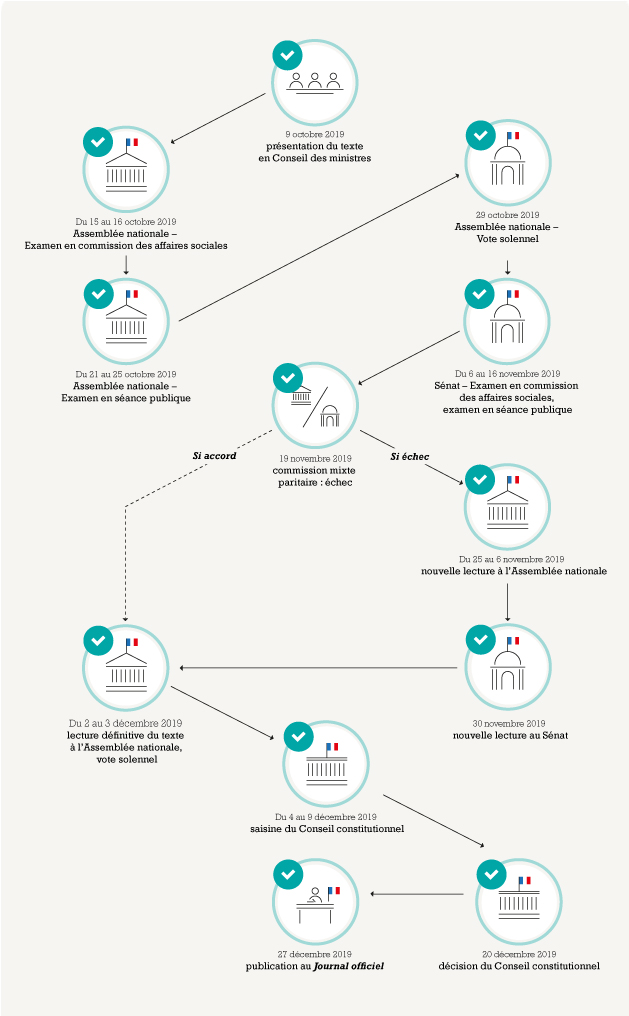
La Loi de financement de la Sécurité sociale (LFSS) pour 2020 a été promulguée le 27 décembre 2020. Le point sur les principales mesures concernant la pharmacie.
Parue au Journal officiel du 27 décembre 2019, la Loi de financement de la Sécurité sociale (LFSS) pour 2020 compte plus de 90 articles, dont une douzaine concerne particulièrement la pharmacie.
Art. 33 – Réforme du financement des hôpitaux de proximité : la LFSS « sécurise, par une garantie pluriannuelle de financement, l’activité de médecine, exercée par tous les hôpitaux de proximité » . Les établissements bénéficieront d’une dotation de responsabilité territoriale, permettant l’accès à des consultations de spécialités, des plateaux techniques et des équipements de télésanté.
Leur financement tiendra aussi compte de leur participation à l’offre de soins au sein d’un territoire et valorisera les liens avec les professionnels exerçant en ville.
Art. 36 – Refonte du modèle de financement des services d’urgence : cet article vise à réformer en profondeur le financement des services d’urgence à compter du 1er janvier 2021, puisqu’il introduit une dotation populationnelle.
Art. 38 – Rénovation de la nomenclature : l’article vise à réviser la nomenclature des actes et prestations pratiqués en ville.
Art. 64 – Contrat d’amélioration de la qualité et de l’efficience des soins (Caqes) et adaptation du dispositif du financement de la qualité : l’article 64 rénove le Caqes signé entre les établissements de santé, l’État et l’Assurance maladie afin de donner plus de cohérence aux priorités fixées en matière de pertinence et d’efficience.
Le dispositif d’intéressement associé à ce contrat est renforcé : afin de mobiliser davantage les services ou les pôles prescripteurs, les établissements pourront récupérer une partie des économies générées dans le cadre de l’expérimentation biosimilaires.
Art. 39 – Prise en charge des dispositifs médicaux : cet article introduit deux nouvelles modalités qui modifient les conditions de prise en charge de certains dispositifs médicaux (DM), notamment les fauteuils roulants : la mise en place d’un référencement sélectif et la remise en état de dispositifs déjà utilisés. Ces mesures visent à favoriser leur accessibilité pour les patients et à réduire le gaspillage de matériel.
Art. 42 – Mesures sur les génériques : l’article 42 permet tout d’abord au pharmacien de délivrer un médicament princeps en l’absence de la mention « non substituable », pour certains médicaments à marge thérapeutique étroite dans des situations particulières qui seront précisées par arrêté.
Il reporte en outre au plus tard au 1er janvier 2022 l’application de la limitation de la base de remboursement en cas de refus de la substitution à deux ans après la publication « du prix de la première spécialité générique du groupe ». La date définitive d’application sera fixée par arrêté.
Art. 42 – Abrogation de la substitution des médicaments biosimilaires par les pharmaciens d’officine : cela fait suite à un rapport de l’ANSM relevant l’impossibilité, pour des questions de traçabilité et de sécurité sanitaire, de mettre en œuvre une substitution au moment de la délivrance du produit.
Art. 43 – Expérimentation de l’utilisation du cannabis thérapeutique : cet article permet à l’État de lancer une expérimentation d’une durée de deux ans pour l’usage médical du cannabis dans certaines indications ou situations cliniques réfractaires aux traitements indiqués et accessibles.
Les conditions de prise en charge, le nombre de patients concernés, les modalités d’importation de production, d’approvisionnement, de prescription et de délivrance par les pharmacies hospitalières et d’officine seront définis par voie réglementaire.
Art. 48 – Lutte contre les pénuries de médicaments : dans la continuité de la feuille de route présentée par la ministre des Solidarités et de la Santé en juillet 2019 afin de lutter contre les pénuries de médicaments, cet article introduit plusieurs mesures :
- obligation pour les industriels de constituer pour tous les médicaments des stocks de sécurité jusqu’à quatre mois en France ou en Europe ;
- obligation d’approvisionnement, aux frais de l’industriel, de solutions alternatives en cas de pénurie ;
- obligation d’information de tout risque de rupture de stock des médicaments d’intérêt thérapeutique majeur (MITM) ;
- renforcement des sanctions financières envers les industriels notamment en cas de défaut de constitution de stock ou de défaut d’information à l’Agence nationale de sécurité du médicament et des produits de santé (ANSM) de situation de rupture ou de risque de rupture.
Art. 47 – Prise en charge des frais liés à la contraception pour l’ensemble des mineures : cet article permet à l’ensemble des assurées mineures de bénéficier de la gratuité sur les contraceptifs remboursables et sur les frais relatifs aux actes et aux consultations liés, en tiers payant. Il garantit également la confidentialité de ces actes.
Art. 65 – Prise en charge des TROD en pharmacie d’officine : l’une des dispositions de l’article 65 instaure la prise en charge des tests rapides d’orientation diagnostique (TROD) en officine.
Art. 65 – Pénalité financière à l’encontre des laboratoires exploitant certains médicaments au conditionnement inadapté : cet article instaure la possibilité d’appliquer une pénalité financière à l’encontre des laboratoires exploitant certains médicaments dont le conditionnement ne serait pas adapté. Il précise en outre les conditions d’octroi des recommandations temporaires d’utilisation par l’ANSM.
Art. 66 – Dérogation à l’article 51 de la LFSS 2018 : cet article complète le champ des expérimentations et dérogations prévues à l’article 51 de la LFSS 2018. Il prévoit en particulier une dérogation afin de permettre le remboursement d’examens de biologie médicale réalisés à la demande du patient sans prescription médicale. Une seconde dérogation prévoit l’extension des lieux et des conditions de prélèvements et de réalisation de la phase analytique des examens de biologie médicale.
Art. 67 – Biologie médicale délocalisée : il entérine le développement, dans les structures de premier recours, de la biologie médicale délocalisée (réalisation des phases préanalytiques et analytiques en dehors d’un laboratoire de biologie médicale), mesure qui avait été annoncée par Agnès Buzyn dans le cadre du plan urgences. Un arrêté fixera les conditions et les lieux de réalisation de la phase préanalytique des examens de biologie médicale délocalisés. S’agissant de la phase analytique de ces examens, un arrêté fixera uniquement les lieux de sa réalisation.